Nein, Sie sind nicht im falschen Film! Hier geht es darum, ob und unter welchen Bedingungen Biofilme für uns Menschen gefährlich werden können. Also: „Film ab“?
Gerade in letzter Zeit wurde ich öfter von Patient:innen nach diesen ominösen Biofilmen gefragt, „von denen man immer hört“. Zeit für die ersehnte Aufklärung:
Biofilme sind Schleimgebilde, in denen sich Mikroorganismen, zum Beispiel Bakterien, „sauwohl“ fühlen. In diesen Verbänden können sich Bakterien nämlich besonders gut organisieren … und somit auch effektiv Antibiotika trotzen!
Dabei finden sich solche Biofilme beileibe nicht nur in unserem Körper, sondern auch in der Natur und z. B. in jeder Wasserleitung. Die Frage nach dem Warum ist schnell geklärt: Besonders gut gefällt den Biofilmen nämlich eine feuchte Umgebung, denn dort können sich die Mikroorganismen am schnellsten vermehren.
Biofilme – von hauchdünn bis massiv
Wie haben wir uns nun einen solchen Biofilm vorzustellen? In der Regel sind sie so dünn, dass sie mit dem bloßen Auge gar nicht erkennbar sind, doch theoretisch können Biofilme bis zu einigen Zentimetern dick werden. Normalerweise besteht ein Biofilm nicht nur aus einer speziellen Bakterien- oder Pilzgattung, sondern beinhaltet einen bunten Mix aus verschiedensten Mikroorganismen. Viren, Bakterien, Pilze oder Algen – alles kann darin fröhlich koexistieren.
In der Biofilmumgebung haben diese es sich gemütlich gemacht, eingebettet in sogenannte extrazelluläre polymere Substanzen, zu einem großen Teil Kohlenhydratstrukturen.
Strategisch optimal geschützt
Diese Zwischenzellsubstanz ist abhängig von den verschiedenen Bedingungen in der jeweiligen Umgebung der Biofilme. Sie ermöglicht einerseits Kommunikation und Stoffaustausch zwischen den Mikroorganismen, übt andererseits auch eine Schutzfunktion aus.
So sind Biofilme z. B. sehr effektiv gegen UV-Strahlung, Schadstoffe und Temperaturveränderungen geschützt. Normale Strategien, um Viren und Bakterien abzutöten – wie z. B. Erhitzen oder der Einsatz von Desinfektionsmitteln – wirken hier also nur bedingt.
Alles für ein schönes Zuhause
Innerhalb eines Biofilms gibt es eine ausgeklügelte Zusammenarbeit. Indem jeder Mikroorganismus das leistet, was er am besten kann, verhilft er dem Biofilm zu besseren Überlebenschancen. Beispielsweise gibt es Gruppen von Bakterien, die Nährstoffe aufspalten und so für andere überhaupt erst zugänglich machen. Andere kümmern sich um eine „schöne Wohnumgebung“ und stellen die extrazellulären polymeren Substanzen her, die praktisch das Zuhause der Mikroorganismen bilden.
Diese effektive Kooperation verschafft den Mikroorganismen des Biofilms einen entscheidenden Vorteil gegenüber einzelnen Bakterien, die sich praktisch überall befinden. Dementsprechend können die Biofilme in unserem Körper auch deutlich mehr Schaden anrichten als einzelne Bakterien!
Wie gefährlich die Biofilme jedoch für unseren Körper werden, hängt von der Zusammensetzung der beteiligten Mikroorganismen ab. Besonders häufig finden sich in Biofilmen beim Menschen die Bakterienarten Pseudonomas, Staphylokokken und Streptokokken.
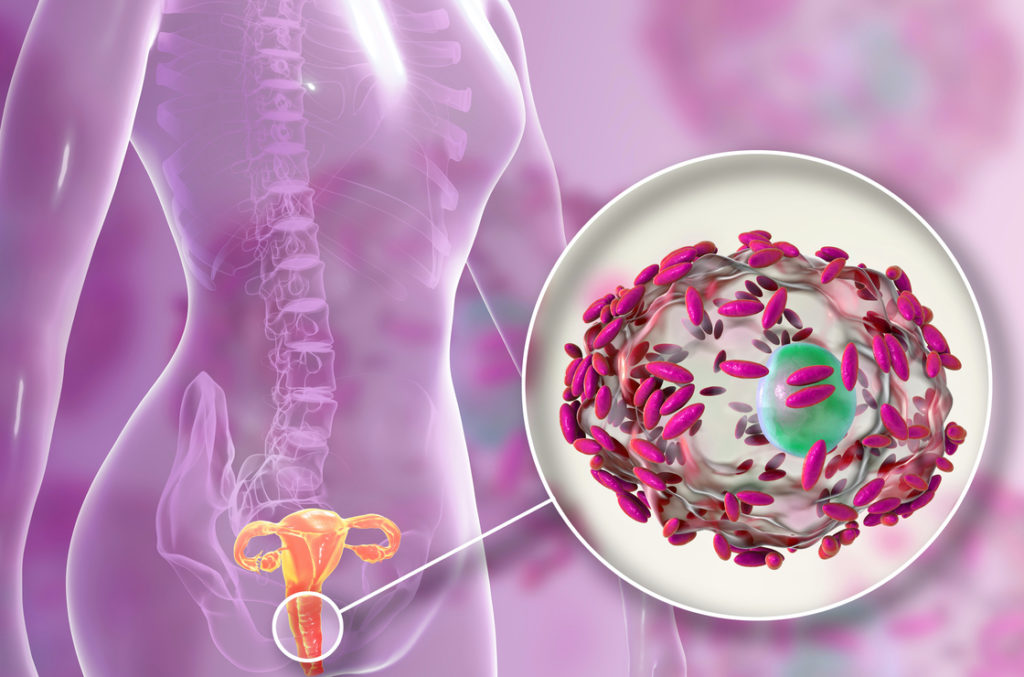
Biofilme im Intimbereich? Nichts, was frau sich wünscht
Einer der beliebtesten Orte für Biofilme ist der Vaginaltrakt, was insofern „vertrackt“ ist, weil dadurch schnell eine bakterielle Vaginose entstehen kann. Wegen ihrer Häufigkeit habe ich dieser Erkrankung schon mal einen ganzen Blog gewidmet:
„Zwei Keimstämme sind wahre „Verdrängungskünstler“, wenn es darum geht, die physiologische Vaginalflora zu verdrängen“
D. Praßler
Besonders berüchtigt ist hier ein Biofilm aus anaeroben Keimen (also solchen, die keinen Sauerstoff mögen). Zwei Stämme haben sich als wahre „Verdrängungskünstler“ erwiesen, wenn es darum geht, die physiologische Vaginalflora zu verdrängen: Gardnerella vaginalis und Atopobium vaginae.
Ist das gesunde Vaginalmikrobiom erst mal erfolgreich in seiner Funktion beeinträchtigt, entstehen schnell unangenehme Gerüche oder gräulicher Ausfluss. Auch die Gefahr, sich mit sexuell übertragbaren Erkrankungen anzustecken oder einen Harnwegsinfekt zu bekommen, ist deutlich erhöht! Ein Biofilm im Intimbereich ist also wirklich nichts, was frau sich wünschen würde.
Wenn schon ein Antibiotikum, dann nicht dieses!
Um gegen den unerwünschten Biofilm und die damit einhergehende bakterielle Entzündung vorzugehen, wird betroffenen Patientinnen häufig das Antibiotikum Metronidazol verschrieben. Das aber ist fatal, denn bei Biofilmen liegt man damit gleich doppelt falsch!
Zum einen sind Antibiotika, wie schon erwähnt, im Angesicht des gut organisierten, wehrhaften Biofilms ziemlich machtlos. Selbst wenn sich die Symptome nach der Antibiotikatherapie kurzzeitig bessern, kehrt die Infektion doch meistens innerhalb einiger Wochen zurück.
Zum anderen ist das in vaginalen Biofilmen häufig enthaltene Atopium vaginae nicht selten resistent gegen Metronidazol. Wenn also zu einem Antibiotikum gegriffen werden soll, um Biofilme zu entfernen, dann bitte ein anderes!
So klappt es auch mit dem Nachbarn
Zum Glück gibt es eine andere Methode, so einen Biofilm auf Dauer loszuwerden. Sie basiert auf der Erkenntnis, dass kein Weg an der Wiederherstellung eines normalen und gesunden vaginalen Mikrobioms vorbeiführt.
Ein Probiotikum hat sich hierbei besonders bewährt: OMNi-BiOTiC® FLORA Plus nutztunterschiedliche Lactobazillenstämme (Milchsäurebakterien) in Milliardenstärke, die sich an der Vaginalschleimhaut ansiedeln und so einen immunologischen Prozess in Gang setzen, an dessen Ende die Auflösung des Biofilmes steht. Sollte jetzt noch ein Antibiotikum nötig sein, kann es die nun ungeschützten pathogenen Keime zumindest teilweise vernichten.
Das Ansiedeln der Bakterien ist ein wichtiger Prozess und gelingt am nachhaltigsten, wenn die Bakterien als Probiotikum oral eingenommen wurden und dann – über den „Nachbarn“ Darm – in das weibliche Mikrobiom gelangen. Vaginale Zäpfchen mit Lactobazillen senken zwar vorübergehend den pH-Wert (das ist gut, denn wir brauchen ein saures Milieu auf all unseren Schleimhäuten), aber sie verlassen die Vagina wieder und siedeln sich nicht an. Das ist ein entscheidender Punkt!
Ich muss Sie, wenn Sie diesen Blog schon länger verfolgen, wohl nicht noch einmal darauf hinweisen, dass grundsätzlich zu jedem Antibiotikum ein Probiotikum wie OMNi-BiOTiC® 10 eingenommen werden sollte. In der Biofilm-Branche heißt es also: bei Problemen im vaginalen Mikrobiom OMNi-BiOTiC® FLORA Plus über drei Monate, bei Antibiotika-Einnahme darüber hinaus OMNi-BiOTiC® 10.
Reizdarmsyndrom durch Biofilm?
Ständige Darmprobleme und immer auf der Suche nach der nächsten Toilette? Ein wirklich schlimmes Leiden für viele meiner Patient:innen. Die meisten hatten eine lange Odyssee hinter sich, bevor es hieß: Endstation „Reizdarm“. Leider bedeutet dies in den meisten Fällen aber nicht, dass dann wirklich etwas gegen die Symptomatik getan würde!
Dafür gibt es Gründe: Ein großes Problem ist nämlich, dass die Mechanismen, die zum Entstehen eines Reizdarms führen, noch nicht genau bekannt sind. Was aber zweifelsfrei immer dazugehört, ist ein aus dem Gleichgewicht geratenes Darmmikrobiom!
Dass bei der Diagnose Reizdarm auch ein im Darm etablierter Biofilm eine Rolle spielt, hat eine Forschergruppe aus Wien gezeigt. Bis zu zwei Drittel der von ihnen untersuchten Probanden mit Reizdarmsyndrom hatten offenbar mit einem solchen Bakterienfilm zu kämpfen.

Mit der Spritzpistole im Anschlag
Doch wie wird man den hartnäckigen Biofilm im Darm los? Eine optimale Methode für alle betroffenen Darmbereiche wurde leider bis heute noch nicht gefunden. Gerade im Dickdarm kann aber durchaus etwas gegen den Bakterienfilm helfen. Genutzt wird hier eine Art endoskopisch nutzbare Spritzpistole, die den Biofilm in diesem Bereich wegspülen kann – klingt lustig, ist aber wohl effektiv.
Neben dieser innovativen Methode gibt es aber doch noch einiges, was man tun kann, um die Reizdarmbeschwerden zu lindern. Warum bei der Wiederherstellung eines gesunden Mikrobioms Probiotika das Mittel der Wahl sind und welche Rolle die Art der Ernährung dabei spielt, können Sie hier noch genauer nachlesen:
Im Mund sind Biofilme nicht per se gefährlich
Da die Mikroorganismen der Biofilme sich bevorzugt in feuchten Gebieten ansiedeln, ist es nicht verwunderlich, dass auch der Mund ein beliebter Ort für Biofilme ist. Auch hier haben wir ein natürlich vorkommendes Mikrobiom, das uns gute Dienste tut. Tatsächlich beherbergt die Mundhöhle – nach dem Darm – mit bis zu 1000 verschiedenen Bakterienstämmen die zweitgrößte Ansammlung von Mikroben in unserem Körper. Die Anzahl der Stämme ist abhängig vom Alter, dem Gesundheitsstatus und der Ernährung.

Doch längst nicht alle Biofilme, die hier entstehen, sind automatisch schlecht für uns: Nachdem wir unsere Zähne geputzt haben und erst einmal deren Besiedelung beseitigt haben, legt sich nämlich ein dünner Biofilm als Schutzschicht über den Zahn. Sind hier nur die normalen Bakterien des oralen Mikrobioms und verschiedene Eiweiße enthalten, funktioniert das wunderbar und schützt unsere Zähne – unter anderem vor Säure.
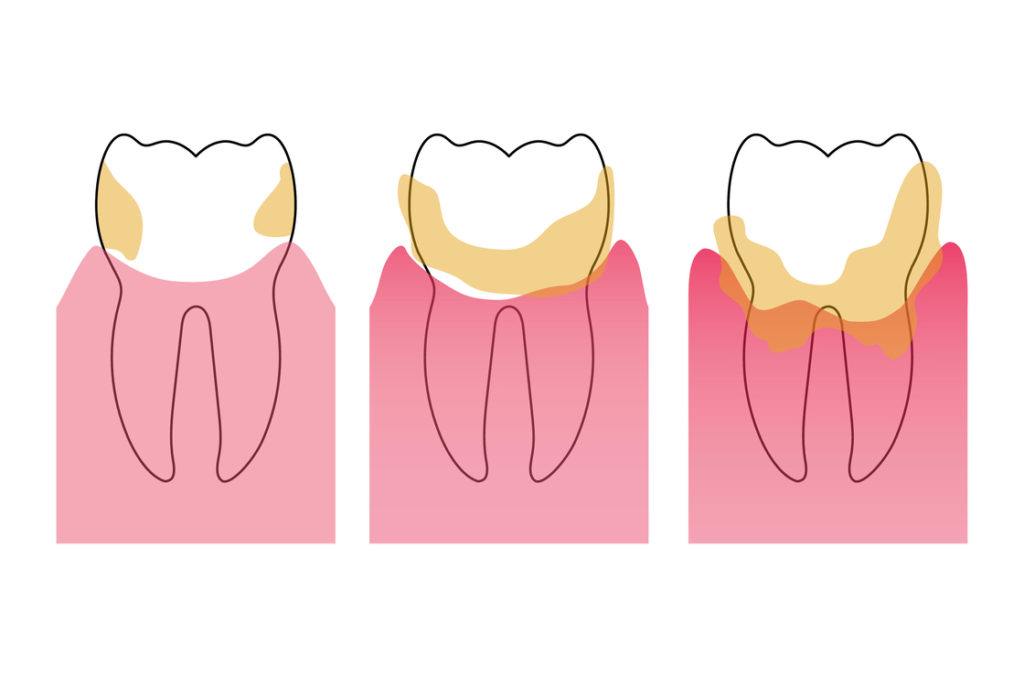
Legen sich allerdings Biofilme mit schädlichen Mikroorganismen über unsere Zähne oder auch auf Zahnimplantate (was besonders häufig passiert), kann dies schnell zu Problemen führen. Gerade dann, wenn wir es mit dem Zähneputzen nicht so genau nehmen, kann sich umso schneller Karies oder Parodontitis entwickeln – keine schöne Erfahrung!
Hast Du Probiotika in den Taschen …
Neben adäquater zahnärztlicher Behandlung empfehlen sich auch hier Probiotika. Die Gabe von aktiven Bakterienstämmen hilft nämlich nicht nur unserem Darm, sondern auch dem oralen Mikrobiom. Durch diese „nützlichen“ Bakterien können pathogene Keime leichter verdrängt werden – selbst wenn sie sich einen Biofilm als Rückzugsort ausgesucht haben.
Mehr dazu lesen Sie hier: https://probiotische-praxis.blog/parodontitis/parodontitis-ursachen/
Tatsächlich gibt es heute schon Verfahren, bei denen ein Probiotikum direkt in die Zahnfleischtaschen gegeben wird. Doch es gibt noch einen einfacheren Weg, das orale Mikrobiom zu stärken: Mit OMNi-BiOTiC® iMMUND – einemProbiotikum zum Lutschen, das zusätzlich Vitamin D enthält – wird der Prozess der Zellteilung in der Mundschleimhaut angeregt. Und je häufiger diese sich regeneriert, desto besser kann die Mundschleimhaut als Barriere gegen unerwünschte Keime fungieren!
Verantwortlich für die hohe Wirksamkeit ist bei diesem Präparat in erster Linie ein Bakterium namens Streptococcus salivarius K12, das sich ursprünglich als besonders effektiv gegen Mittelohrentzündung erwiesen hat. Welch positive Wirkung es aber auch im gesamten Mund- und Rachenraum ausübt, habe ich hier im Detail beschrieben:
Bei künstlichen Gelenken droht Gefahr
Neben Zahnimplantaten wirken auch alle anderen neu in den Körper „eingebauten“ Strukturen wie z. B. künstliche Gelenke, Herzschrittmacher oder Herzklappen wie ein Magnet für Biofilme – mit schwerwiegenden Folgen: Nicht selten hat dies so gravierende Auswirkungen auf den Gesundheitszustand der Patient:innen, dass die Implantate ausgetauscht werden müssen!
Leider hat man bis heute noch keine effektive Lösung für dieses Problem gefunden, aber es wird mit Hochdruck daran gearbeitet, Methoden zu entwickeln, mit denen sich Biofilme auf implantierten Strukturen bekämpfen lassen – vor allem die Suche nach weitgehend mikroorganismenresistenten Materialien gehört dazu.
Eines können Biofilme nicht gut riechen
Während die Erforschung der Biofilme noch längst nicht abgeschlossen ist, hat sich ein Mittel gegen diese Verbände aus Mikroorganismen bewährt: ätherische Öle. Je nach Bakterienart gibt es verschiedene natürliche Wirkstoffe, die antibakteriell wirken. Ein Beispiel ist Thymianöl, das sehr effektiv gegen resistente Infektionen durch Staphylococcus aureus wirkt.
Auch aus Meerrettich, Lavendel, Eukalyptus, Wacholder oder Bohnenkraut hergestellte ätherische Öle können gegen manche Bakterienstämme eingesetzt werden. Untersuchungen haben gezeigt, dass der Einsatz solcher Öle nicht nur die Bildung von Biofilmen hemmt, sondern auch bereits etablierte Biofilme wirksam bekämpfen kann.
Mit Öl gegen die Kolonisatoren

Während herkömmliche Antibiotika häufig nur an der Oberfläche der Biofilme kratzen und den größten Teil der Mikroorganismen-Kolonie unbeschadet lassen, konnte gezeigt werden, dass es ätherischen Ölen durchaus gelingt, den ganzen Film anzugreifen.
Je nach Fall können die ätherischen Öle also zusätzlich zu Antibiotika eingesetzt werden, wenn deren Wirkung nicht allein ausreicht. Angewendet werden sie zum Beispiel häufig als Mundspülung für Parodontitis-Patient:innen.
Biofilme in der Kritik
Einen Oscar wird es also für die heute unter die Lupe genommenen Biofilme nicht geben. Aber die „Goldene Himbeere“ für eine schlechte Performance haben sie auch nicht verdient, denn ihre hohe Widerstandsfähigkeit und die perfekt organisierte Zusammenarbeit der Mikroorganismen können sich wirklich sehen lassen.

Zum Glück gibt es mit kombinierten Probiotika- und Antibiotikatherapien sowie ätherischen Ölen mehrere gute Ansätze, unerwünschte Biofilme aus unserem Körper zu verbannen. Und der aktuelle Forschungstand gibt Anlass zur Hoffnung, dass uns schon bald weitere Methoden zur Verfügung stehen werden!
Sie sehen: In diesem Zusammenhang heißt es in aller Regel „Film ab“. Ich hoffe, Sie sehen das auch so. Machen Sie’s gut und bleiben Sie gesund!
Herzlich, Ihre
Dagmar Praßler
Titelbild: © AlexLMX / shutterstock
Biofilm entfernen
In meinen Blogs beschreibe ich Erfahrungen aus meiner Praxis, insbesondere den Verlauf einiger konkreter Behandlungen. Ich weise darauf hin, dass die beschriebenen Verläufe Einzelfälle sind und keine allgemein verbindlichen Rückschlüsse daraus gezogen werden können. Andere Menschen können anders reagieren, auch wenn sie die gleiche Behandlung erfahren. Es handelt sich um meine subjektiven Wahrnehmungen, ein Heilversprechen ist darin nicht zu sehen. Bei Beschwerden sollten Sie einen Arzt oder Heilpraktiker aufsuchen. Bei meinen Blogs handelt es sich ausschließlich um redaktionelle Beiträge. Neben den beschriebenen Produkten gibt es noch weitere von anderen Herstellern.







